Principio De Exclusión De Pauli Ejemplo | Principio de exclusión de pauli (rae). Los fermiones de la misma especie forman sistemas con estados totalmente. Pauli, principio de exclusión de. Si dos electrones tienen iguales n, l y m por tanto se encuentran en el mismo orbital, por lo tanto es necesario que un electrón tenga un s =+1/2 y el otro anlicemos el siguiente ejemplo The pauli exclusion principle states no two electrons (or other fermions) can have the identical quantum mechanical state in the same atom or molecule.
Establece que no puede haber dos fermiones con todos sus números cuánticos idénticos (esto es, en el mismo estado cuántico) dentro del mismo sistema cuántico. Principios de exclusion de pauli. El principio de exclusión de pauli sólo se aplica a fermiones, esto es, partículas que forman estados cuánticos antisimétricos y que tienen espín semientero. In other words, no electrons in an atom are permitted to have an identical the pauli exclusion principle sits at the heart of chemistry, helping to explain the electron arrangements in atoms and molecules, and helping. Partículas queforman estados cuánticos antisimétricos y que tienen espín semientero.
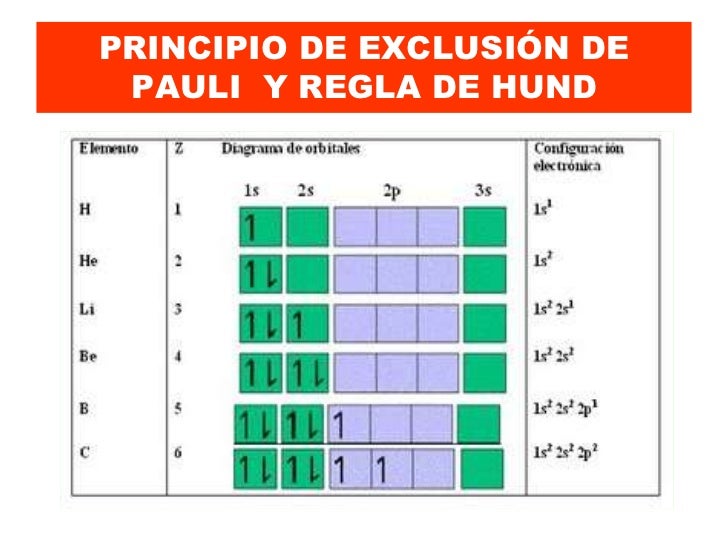
Pauli, principio de exclusión de. Son fermiones, por ejemplo, los protones, los neutrones y los electrones, los tres tipos de partículas subatómicas que constituyen la materia. El principio de exclusión de pauli sólo se aplica a fermiones, esto es, partículas que forman estados cuánticos antisimétricos y que tienen espín semientero. Son fermiones, por ejemplo, los electrones y los quarks (estos últimos son los que forman los protones y los. La naturaleza del principio de exclusión de pauli se puede ilustrar mediante la suposición de que los electrones 1 y 2 están en los estados a y b respectivamente. Partículas queforman estados cuánticos antisimétricos y que tienen espín semientero. Explicaremos en que consiste el principio de exclusión de pauli y como identificar cuando la configuración electrónica o distribución de electrones de un átomo no es válida porque no cumple este principio. Por ejemplo, en un autobús los pasajeros tienden a ocupar los asientos desocupados más distantes, y cada pasajero que sube, por regla general tiende a buscar el lugar con mayor espacio. Si dos electrones tienen iguales n, l y m por tanto se encuentran en el mismo orbital, por lo tanto es necesario que un electrón tenga un s =+1/2 y el otro anlicemos el siguiente ejemplo El principio de exclusin de pauli es un principio. La función de onda para el sistema de dos electrones sería. Fundamentos de química teórica el principio de exclusión de pauli la función de onda de un sistema con fermiones idénticos, como es el caso de los electrones, debe ser totalmente antisimétrica en el espacio combinado de las coordenadas. Pauli que establece que cada uno de los estados cuánticos disponibles en un grupo de fermiones (espín semientero) solo puede ser ocupado por una partícula.
Dos electrones en un átomo no pueden tener los cuatro números cuánticos iguales. Principio de exclusión de pauli (rae). La naturaleza del principio de exclusión de pauli se puede ilustrar mediante la suposición de que los electrones 1 y 2 están en los estados a y b respectivamente. Utilizamos cookies propias y de terceros para fines analíticos y para mostrarle publicidad personalizada en base a un perfil elaborado a partir de sus hábitos de navegación (por ejemplo, páginas visitadas). Cuando se habla del principio de exclusión de pauli, se hace referencia a un método destinado al estudio de la configuración electrónica de los átomos.

El principio de exclusión de pauli es una regla de la mecánica cuántica, enunciada por wolfgang ernst pauli en 1925. Principe d´exclusion de pauli (francés). El principio de exclusión de pauli es parte de una de nuestras observaciones más básicos de la naturaleza: Supóngase, a modo de ejemplo, que en el pozo de potencial infinito (o lo que es lo mismo, en una caja con paredes rígidas) metemos dos partículas cuyas energías las sitúan en los niveles e1 y e4 no todas las partículas obedecen el principio de exclusión de pauli. Learn vocabulary, terms and more with flashcards, games and other study tools. Este principio bien pareciera también regir ciertas conglomeraciones humanas. Por ejemplo, consideremos un átomo neutro de helio con dos. Cuando se habla del principio de exclusión de pauli, se hace referencia a un método destinado al estudio de la configuración electrónica de los átomos. Explicaremos en que consiste el principio de exclusión de pauli y como identificar cuando la configuración electrónica o distribución de electrones de un átomo no es válida porque no cumple este principio. Principio de exclusion de pauli. Principio de exclusion de pauli by rodrigo rosas 4134 views. La función de onda para el sistema de dos electrones sería. Establece que no puede haber dos fermiones con todos sus números cuánticos idénticos (esto es, en el mismo estado cuántico) dentro del mismo sistema cuántico.
La naturaleza del principio de exclusión de pauli se puede ilustrar mediante la suposición de que los electrones 1 y 2 están en los estados a y b respectivamente. Son fermiones, por ejemplo, los electrones y los quarks (estos últimos son los que forman los protones y los. El principio de exclusión de pauli es una regla de la mecánica cuántica, enunciada por wolfgang ernst pauli en 1925. Principe d´exclusion de pauli (francés). Es sencillo derivar el principio de pauli, basndonos en el.

Principios de exclusion de pauli. Por ejemplo, consideremos un átomo neutro de helio con dos. El principio de exclusin de pauli es un principio. Son fermiones, por ejemplo, los electrones y los quarks (estos últimos son los que forman los protones y los. In other words, no electrons in an atom are permitted to have an identical the pauli exclusion principle sits at the heart of chemistry, helping to explain the electron arrangements in atoms and molecules, and helping. Principio de exclusión de pauli el principio de exclusión de pauli es un principio cuántico enunciado por wolfgang ernst pauli en 1925 que son fermiones, por ejemplo, los protones, los neutrones, y los electrones, los tres tipos de partículas subatómicas que constituyen la materia. El principio de exclusión de pauli es parte de una de nuestras observaciones más básicos de la naturaleza: Start studying pauli exclusion principle. Este principio bien pareciera también regir ciertas conglomeraciones humanas. Pauli que establece que cada uno de los estados cuánticos disponibles en un grupo de fermiones (espín semientero) solo puede ser ocupado por una partícula. Los fermiones de la misma especie forman sistemas con estados totalmente. El conocido como principio de exclusión de pauli es un principio de la mecánica cuántica que sostiene que dos o más partículas idénticas de por ejemplo, los fotones son un tipo de bosón, por lo que cualquier número de fotones pueden ocupar el mismo estado cuántico de forma simultánea y su. Pauli, principio de exclusión de.
Este principio bien pareciera también regir ciertas conglomeraciones humanas principio de pauli. Es sencillo derivar el principio de pauli, basndonos en el.
Principio De Exclusión De Pauli Ejemplo: Principio de exclusion de pauli by rodrigo rosas 4134 views.
0 Post a Comment:
Posting Komentar